Polyphenole
Polyphenole
Polyphenole sind Substanzen des Polyketidstoffwechsels, die im Pflanzenreich verschiedenste Funktionen erfüllen: sie bieten Schutz vor Pathogenen, Mikroorganismen, UV-Einwirkung und Bedingungen des oxidativen Stress. Zum Beispiel halten Tannine Herbivore davon ab, die adstringierenden Früchte zu fressen. Phenolische Komponenten wie Salicylsäure fungieren als Signalmoleküle und Lignin sorgt für mechanische Stützung des Zytoskeletts.
Ein phenolisches Molekül ist oft charakteristisch für eine bstimmte Pflanzenart.
Die Unterteilung der Polyphenole erfolgt anhand der Struktur ihres Kohlenstoffskeletts in Phenolsäuren, Flavonoide, Stilbene und Lignane.
Phenolsäuren kommen in vielen Lebensmitteln vor; am häufigsten findet man Kaffesäure und Ferulasäure. Die Kaffeesäure liegt oft als Ester vor, der bekannteste Kaffeoylester ist die Chlorogensäure (bis 150 mg pro 200 ml Kaffee). Die am häufigsten vorkommenden Polyphenole in unserer Nahrung stellt die Klasse der Flavonoide dar.
Klassifizierung der Flavonoide
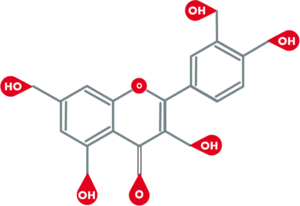
Flavonoide gehören zu der Klasse der Phenylchromanderivate, deren Grundgerüst das Flavan (2-Phenylchroman) ist. Die über eine C3-Brücke verbundenen aromatischen Ringe sind unterschiedlich substituiert: Anhand des Substitutionsmusters am C-Ring werden die Flavonoide in die Flavanole (3-Hydroxyflavane), Flavandiole (3,4-Dihydroxyflavane), Flavanone (4-Oxoflavane) und Flavone (3-Oxoflav-2-ene) unterteilt.
Die Flavanole werden auch als Catechine bezeichnet, besitzen eine Catecholstruktur am B-Ring und liegen zum Teil an Gallussäure gebunden vor. Proanthocyanidine sind zu Di- bis Oligomeren kondensierte Flavanole. Galloylierte Flavanole bilden die Prodelphinidine, bestehen sie nur aus Catechin- und Epicatechin-Untereinheiten, werden sie als Procyanidine bezeichnet.
Vorkommen
Mit der Nahrung, insbesondere Früchten und Getränken, werden pro Tag durchschnittlich 1g Polyphenole aufgenommen; ein Drittel davon stellen Phenolsäuren dar, die anderen zwei Drittel machen die Flavonoide aus. Die Hauptvertreter der Flavonoide in der Nahrung sind die Flavanole (Catechine plus Proanthocyanidine), Anthocyanine und deren Oxidationsprodukte . Das Vorkommen der Gallate und Gallocatechine ist fast ausschließlich auf Tee beschränkt. Ein Aufguss grünen Tees enthält ca. 1 g Catechine pro Liter , wobei schwarzer Tee aufgrund der Fermentation noch ca. 50% des Catechin-Gehaltes aufweist.
(+)-Catechin-Konzentrationen sind besonders hoch in Bohnen, roten Trauben, Aprikosen und Erdbeeren; (-)-Epicatechin ist in hohen Konzentrationen in Äpfeln, Brombeeren, Bohnen, Kirschen, roten Trauben, Birnen, Himbeeren und Schokolade zu finden. Pflaumen, Avocados, Erdnüssen, Curry und Zimt enthalten A-Typ Procyanidine, B-Typ Procyanidinen sind besonders in Kakao, Brombeeren, Kirschen, Feigen, Pflaumen, roten Trauben, Wein und Äpfeln anzutreffen.
In den roten Trauben des Weins (Vitis vinifera) sind vornehmlich Procyanidine vom B-Typ anzutreffen, die monomeren Untereinheiten machen nur einen geringen Anteil aus; der höchste Flavanol-Anteil ist in den Kernen zu finden, während in der Schale in erster Linie das Phytoalexin Resveratrol nachzuweisen ist.
In Zitronen (Citrus limonium) und Orangen (Citrus sinensis) sind in erster Linie Hesperidin und Narirutin anzutreffen; Naringin ist das Hauptflavonoid der Grapefruit (Citrus paradisi) und verantwortlich für den bitteren Geschmack. In einem Liter Orangensaft sind ca. 450 mg Hesperidin und 95 mg Narirutin enthalten.
Wirkung von Polyphenolen
Der tägliche nahrungsbedingte Konsum der Flavonoide ist deutlich höher als der anderer Mikronährstoffe (z.B. antioxidativer Vitamine und Provitamine), ein Aspekt, der das Interesse der Wissenschaft weckte und zu zahlreichen in-vivo und in-vitro Studien führte. Das vermutlich am besten untersuchte Flavonoid ist das Flavonol Quercetin, welches glykosidisch gebunden vor allem in Ginkgo biloba, Crataegus-Arten und seinem Namensgeber Quercus ssp. (Eiche) zu finden ist. Epidemiologische Studien belegen eine Korrelation zwischen erhöhtem Flavonoid-Konsum und einem verminderten Risiko für bestimmte Krebserkrankungen, Schlaganfälle, und koronare Herzerkrankungen. Neuere Untersuchungen konnten ähnliche Effekte für Procyanidine und deren Flavanol- Untereinheiten aufzeigen.
Die Eigenschaften der Flavanole und Procyanidine können als antiinflammatorisch, vasoprotektiv, antibronchokonstriktorisch, antiarteriosklerotisch und antikarzinogen charakterisiert werden. Meist liegen den Effekten komplexe Wirkmechanismen zugrunde.
In der Hautpflege ist der antiinflammatorische und antioxidative Effekt der Polyphenole am wichtigsten.
Oxidativer Stress resultiert aus einem Ungleichgewicht zwischen Oxidantien, so genannten reaktiven Sauerstoff (ROS)-Spezies und antioxidativen Abwehrsystemen.
Lipide, Proteine und Nukleinsäuren sind Ziele von ROS, die durch Oxidationsreaktionen ihre Funktion teilweise oder auch ganz verlieren. Ein Beispiel für diese Schädigung ist die Lipidperoxidation, die zum Verlust dynamischer Eigenschaften der Zellmembran führen kann.
Die Stärkung der antioxidativen Verteidigungssysteme wird als eine Möglichkeit in der Prävention von Hautkrankheiten gesehen.
Viele Flavonoide, im Besonderen Epicatechin, weisen antioxidative Wirkungen auf.
Aufgrund ihrer Struktur haben Flavanole wie alle Polyphenole reduzierende Eigenschaften und können radikalisch ablaufende Kettenreaktionen (z.B. Lipidperoxidation) unterbrechen.
Sie interagieren mit anderen Antioxidantien wie a-Tocopherol (Vitamin E), b-Carotin (Provitamin A) oder Ascorbinsäure (Vitamin C) und schützen, als Bestandteil des antioxidativen Netzwerks, Zellbestandteile vor dem Angriff von ROS. Die chemische Struktur bestimmt ihr Redox-Potential, wobei Polyphenole mit zwei vicinalen Hydroxygruppen am aromatischen Rest bessere antioxidative Eigenschaften besitzen, als solche mit nur einer freien Hydroxygruppe.
Quellen:
- Teuscher EM, M.; Lindequist, U.: Biogene Arzneistoffe. 1997, 5. Auflage.
- Interventionsstudien und in-vitro-Untersuchungen zum Effekt von Polyphenolen und Omega-3-Fettsäuren auf Endothelialfunktionen und Hautphysiologie, Dissertation; Karin Isolde Neukam, 2006
- Scalbert A, Williamson G: Dietary intake and bioavailability of polyphenols. J Nutr 2000, 130:2073S-2085S.
- Gu L, Kelm MA, Hammerstone JF, Beecher G, Holden J, Haytowitz D, Prior RL: Screening of foods containing proanthocyanidins and their structural characterization using LC-MS/MS and thiolytic degradation. J Agric Food Chem 2003, 51:7513-7521.
- Rice-Evans CA, Miller NJ, Paganga G: Structure-antioxidant activity relationships of flavonoids and phenolic acids. Free Radic Biol Med 1996, 20:933-956