Phytosqualan
Die Fakten zum Phytosqualan
Phytosqualan bzw. Squalan (INCI: Squalane; IUPAC Name: 2,6,10,15,19,23-hexamethyltetracosane; CAS 111-01-3; wird als Inhaltsstoff in der Kosmetik sehr geschätzt. Im Reinzustand ist es ein flüssiges, farbloses, geruchloses und geschmackloses Kohlenwasserstofföl mit guter physikalischer und chemischer Stabilität. Die Eigenschaften zeigen sich in dem hohen Siedepunkt von 210-215 °C (bei 1 torr Druck) und der beträchtlichen Resistenz gegen chemische Oxidation, die Konservierungsmittel überflüssig macht. Squalan kommt in kleinen Mengen in den Lipidschichten der Haut vor; gemeinsam mit seiner Vorstufe Squalen verhindert es Feuchtigkeitsverlust und trägt zur Geschmeidigkeit und Elastizität der Haut bei. Mit seinem sensorischen Profil, seiner Biokompatibilität mit der Haut, seiner chemischen und physikalischen Stabilität und seiner feuchtigkeitsspendenden Wirkung ist es zu einer Lieblingsingredienz der Kosmetikentwickler geworden. Betrachtet man seine technischen Eigenschaften, überzeugt es mit seiner guten Emulgierbarkeit, seiner exzellenten Dispersionsbereitschaft und Kompatibilität mit anderen Inhaltsstoffen. Es ist löslich in allen gängigen kosmetischen Grundlagen und kann ohne Einschränkungen in allen Formulierungstypen eingesetzt werden. Nach der Entfernung von Verunreinigungen, die je nach Herkunft und Typ in unterschiedlichen Mengen vorkommen können, ist es völlig untoxisch und irritationsfrei.
Herkömmliche Quellen von Squalan bzw. Phytosqualan
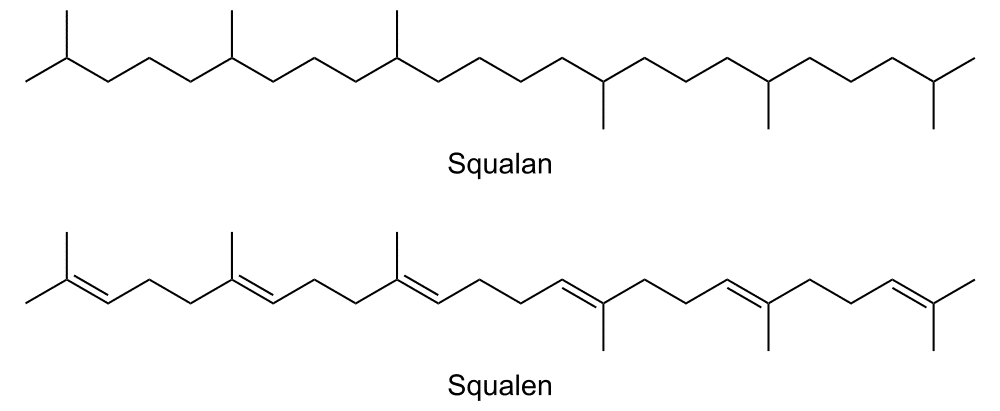
Herkömmlicherweise wird Squalan mittels katalytischer Hydrierung von Squalen (6E,10E,14E,18E-2,6,10,15,19,23- hexamethyltetracosa-2,6,10,14,18,22-hexaene) gewonnen. Squalen ist ein natürlicher Triterpen-Kohlenwasserstoff und eines der wichtigsten Lipide der menschlichen Hautzellen. Es wird in den Talgdrüsen gebildet; sein Anteil an der Gesamtlipidmenge macht hier bis zu 13% aus.Seine Konzentration ist von Hautpartie zu Hautpartie verschieden; die Sekretionsmenge unterscheidet sich zudem von Mensch zu Mensch und reicht von 125 mg bis 475 mg pro Tag.Squalen findet sich auch in Pflanzen, Prokaryoten, Hefe und Mikroalgen.
Für die kommerzielle Nutzung wurde Squalen traditionell aus dem Lebertran des Tiefseehais gewonnen. Das Fischleberöl hat in China, Japan und Korea als Gesundheitsnahrung eine lange Geschichte. Das Haifischleberöl wurde bereits Mitte des 16. Jahrhunderts in einem chinesischen Handbuch über traditionelle Heilmittel erwähnt. Anfang des 20. Jahrhunderts gelang es Marcelet, Chapman und Tsujimoto unabhängig voneinander, einen mehrfach ungesättigten Kohlenwasserstoff aus Haifischleberöl zu isolieren.Tsujimoto, Chemiker auf dem Gebiet der Öle und Fette am Industrieforschungsinstitut in Tokio, entschlüsselte die Formel korrekt als C30H50 und nannte sie Squalen, in Bezugnahme auf die Tatsache, dass Haie zur Familie der Squalidae gehören. 1931 veröffentlichte der Nobelpreisträger von 1937, Paul Karrer an der Universität von Zürich, Schweiz, die komplette chemische Synthese und legte damit den eindeutigen Beweis der chemischen Struktur vor. Aufgrund der zahlreichen Doppelbindungen galt Squalen zunächst als nicht ausreichend stabil für die breite praktische Anwendung, bis Sebastien Sabetay von der französischen Firma Laserson & Sabetay um 1950 auf die Idee kam, es durch Hydrierung zu Squalan bzw.
Perhydrosqualen, wie es damals genannt wurde, umzuwandeln. Dadurch wurde die kommerzielle Nutzung der Substanz als wichtiger kosmetischer Inhaltsstoff möglich.
Ende der 1970er brachte das japanische Unternehmen Kuraray erstmals vollständig synthetisch hergestelltes Squalan auf den Markt. Es war das Produkt der basenkatalysierten Reaktion von 1,3-butadiyne, einem Nebenprodukt der Acetylensynthese aus natürlichem Gas, und zwei Molekülen Geranylaceton – ein Molekül, das tonnenweise für die Synthese von Isophytol, einem Zwischenprodukt in der Herstellung der Vitamine E und K1, und anderer Terpenoide erzeugt wird – mit anschließender Hydrierung des resultierenden Addukts. Trotz des hohen Reinheitsgrades verhinderten die Kosten des Rohstoffes, die auf den vielstufigen Herstellungsprozess zurückzuführen waren, seinen Einsatz in der Kosmetik im großen Stil.
Phytosqualan aus Olivenöl
Squalen kommt in kleineren Mengen in vielen Pflanzenölen vor, beispielsweise in Olivenöl mit einem Gehalt von 0,2-0,5%. Tatsächlich wurde, bevor präzisere Analysemethoden wie Gas- oder Flüssigchromatografie möglich waren, einigen Olivenölen Squalen routinemäßig zugesetzt, um ihren Wert zu steigern, da die Qualität anhand des Squalengehalts bestimmt wurde. Squalen ist auch Bestandteil von Palmöl; sein Gehalt im Palmfettsäuredestillat (PFAD) beträgt bis zu 0,8%, im unverarbeiteten Öl 0,06-0,1%. Das Öl von Amaranthsamen enthält 6-8% Squalen; andere Pflanzenöle enthalten ebenfalls Squalen.
Der Squalengehalt des Olivenöls liegt zwar üblicherweise unter 0,5%; im Unverseifbaren des Öls können aber Konzentrationen von 60-75% vorliegen. Die direkte Gewinnung erschien jedoch bis in die 1980er unwirtschaftlich. Dann ließen sich mehrere spanische Firmen ihre Verfahren patentieren, mit denen sie Squalen aus den Rückständen, die bei der Ölgewinnung aus den Oliven anfallen, extrahieren und raffinieren konnten.Schließlich konnte Hispano Quimica S.A. – das 2000 von Cognis und 2010 von BASF übernommen wurde – “Phytosqualan” bzw. phytosqualane aus Olivenöl-Deodorizer-Destillaten (OODD) auf den Markt bringen. Das konzentrierte Abfallprodukt, das im letzten Schritt der Olivenölraffinierung anfällt, enthält bis zu 30% Squalen. Verbesserungen dieser Technologie wurden schließlich patentiert.
Risiken mit Squalan
In Anbetracht der vielen Quellen, aus denen der Rohstoff Squalen stammt, enthält selbst 100% reines Squalan einige Verunreinigungen. Im Squelen vom Hai können Umweltschadstoffe enthalten sein, z.B. polychlorierte Biphenyle (PCB), Dioxine und Schwermetalle, die sich als Biokonzentrate in der Leber anreichern. Außerdem enthält Squalan Unreinheiten , die sich bei der Biosynthese ansammeln, wie gering flüchtige Triacylglycerine und Glycerylether und bis zu 0,1% C19 Kohlenwasserstoff-Pristan mit hohem Irritationspotenzial. Squalen aus dem Abfall der Olivenölgewinnung kann mit Nebenprodukten der Verarbeitung kontaminiert sein, wie Pflanzenwachse, freie Fettsäuren, Phytosterole und Neutralisierungsnebenprodukte. Aufgrund solcher Verunreinigungen ist die Reinigung des Rohstoffes Squalen und/oder der Squalan-Endprodukte enorm wichtig, um die sichere Anwendung in der Kosmetik zu gewähren.
Wie auch bei anderen natürlichen Rohstoffen ist die Verfügbarkeit von Squalan mit Unwägbarkeiten der Witterung und der Ernte verbunden. Hinzu kommt, dass Squalan mit den Kampagnen zum Schutz des gefährdeten Hais, der zur Squalan-Herstellung genutzt wurde, ins Kreuzfeuer der Kritik geraten ist. Eine Kampagne von Oceana im Jahr 2005 war schließlich ausschlaggebend dafür, dass sich mehrere Kosmetikhersteller öffentlich verpflichteten, die Verwendung von Hai-Squalan in ihren Produkten zu stoppen bzw. auslaufen zu lassen.
Wiederholte Kampagnen haben das Thema seitdem immer wieder “aufgefrischt”, um den Druck auf die Kosmetikunternehmen aufrechtzuerhalten.Eine Aktion der Environmental Justice Foundation Ende 2013 zielte auf den „Schwarzmarkt“ für Hai-Squalan, das als aus Oliven gewonnenes Squalan angeboten bzw. mit solchem vermischt wurde – und das, obwohl mittels analytischer Tests eine Unterscheidung möglich istund die Auflistung der Inhaltsstoffe auf den Produkten entsprechend auf Hai-Squalan hinweisen muss.
Biotechnologische Ansätze zur Gewinnung von Phytosqualan
Erst in jüngerer Zeit bieten Fortschritte in der Biotechnologie Lösungen für diese Probleme und machen es möglich, reine, stabile Produkte in großem Rahmen zu geringen Kosten und aus erneuerbaren Quellen herzustellen. Während bereits in den 1920ern vermutet wurde, dass das Squalen im Isopren-Pfad, der schließlich zu den Steroiden im menschlichen Körper führt , eine Rolle spielt, wurde der Nachweis dafür erst 1964 von Konrad Bloch erbracht. Er entdeckte die Biosynthese des Cholesterins und wurde für seine Arbeit mit dem Nobelpreis geehrt.
Ein neuer Ansatz auf der Basis des Isoprenoid-Pfades beschäftigt sich mit der kommerziellen Herstellung von Phytosqualan aus fermentierbaren Zuckern. b-Farnesen, die natürliche Vorstufe von Squalen, wird in industriellem Maßstab durch Fermentation unter Verwendung der gewöhnlichen, nicht pathogenen Hefe Saccharomyces cerevisiae hergestellt. Die Hefe wird vollständig entfernt, anschließend findet eine einfache chemische Bindung statt, die natürlichen Prozessen ähnelt. Dadurch wiederum erübrigt sich die Isolierung von lipophilem und oxidativ instabilem Squalen aus der Fermentationsbiomasse. Die bekannten Technologien zur Hydrierung und Reinigung können dann eingesetzt werden, um Phytosqualan von hoher Reinheit zu gewinnen. Abb. 2 skizziert das Verfahren.
Flussdiagramm des Prozesses zur Gewinnung von Phytosqualan aus Zucker
Dieses Herstellungsverfahren bietet mehrere Vorteile. Es ist ein erneuerbarer Prozess auf Biobasis. Es ist vom U.S. Department of Agruculture (USDA) als 100% biologisch basiert zertifiziert und von Ecocert anerkannt. Es ist robust und reproduzierbar und stellt zusammen mit der Verfügbarkeit des Ausgangsstoffes die zuverlässige und nachhaltige Produktion von Phytosqualan sicher. Der streng kontrollierte Herstellungsprozess garantiert Chargenkonsistenz sowohl hinsichtlich der chemischen als auch der sensorischen Eigenschaften, wie Geruch und /oder Farbe.
Da der in dem chemischen Prozess eingesetzte Ausgangsstoff β-Farnesen im Gegensatz zu natürlichem Squalen, das Verunreinigungen enthalten kann, ein Kohlenwasserstoff von hoher Reinheit ist, sind die Produkte und Nebenprodukte dieses Prozesses ebenfalls reine Kohlenwasserstoffe.
Zusammensetzung des aus Zucker gewonnenen Phytosqualans
Name Gehalt in % Bemerkung
Phytosqualan 92-94
Isosqualan 3-5
Monocyclosqualan 1-3
Hemisqualane (C15) 0-1
Sesquisqualan (C45) 0-1
Phytosqualan – nachhaltige Gewinnung aus Zuckerrohr
Die Geschichte der Herstellung von Squalan zw. Phytosqualan und seiner Entwicklung und Vermarktung als kosmetischer Inhaltsstoff war von den Unwägbarkeiten hinsichtlich der Verfügbarkeit und Qualität der traditionellen natürlichen Quellen, den Kosten der chemischen Verarbeitung und den Unzulänglichkeiten früherer fermentationsbasierter Techniken bestimmt. Dank der modernen Biotechnologie konnten die Enzym-katalysierten chemischen Reaktionen, wie sie in der Natur vorkommen, nachgebildet und mit herkömmlichen chemischen Prozessen gekoppelt werden, um eine qualitativ hochwertige Quelle für erneuerbares Phytosqualan zu schaffen. Der Prozess basiert auf b-Farnesen, einem Fermentationsprodukt der Hefe Saccharomyces cerevisae, und nutzt eine chemische Reaktion zur reproduzierbaren Herstellung von Phytosqualan, das geruchlos und stabil ist und in einer chargenkonsistenten Zusammensetzung von >99% C30 Kohlenwasserstoffmolekülen verfügbar ist. Das resultierende Zucker-Phytosqualan bietet hohe Qualität und ist in seiner Leistung dem vom Hai gewonnenen Squalan vergleichbar, stammt im Unterschied zu diesem jedoch aus einer erneuerbaren Quelle. Aufgrund dieses fortschrittlichen Herstellungsverfahrens kann erneuerbares Phytosqualan in kosmetischen Formulierungen eingesetzt werden, ohne dass mangelnde Verfügbarkeit oder starke Qualitätsschwankungen Probleme bereiten. Wenn Sie Ihre kosmetischen Produkte ebenfalls mit diesem hauteigenen Lipid vermarkten möchten, sprechen Sie uns gerne an.
Quellen
- S-K Kim and F Karadeniz,Biological importance and applications of squalene and squalane, in Advances in Food and Nutrition Research, vol 65, S-K Kim, ed, Elsevier, Amsterdam, ch14 (2012) pp 223-233
- Final report on the safety assessment of squalaneand squalene, Int J Toxicol 1 37-56 (1982)
- KR Smith and DM Thiboutot,Thematic review series: Skin lipids. Sebaceous gland lipids: Friend or foe? J Lipid Res 49 271-281 (2008)
- RS Greene, DT Downing, PE Pochi and JS Strauss, Anatomical variation in the amount and composition of human skin surface lipid, J Invest Dermatol 54 240-247 (1970)
- T Nikkari, PH Schreibman and EH Ahrens, Jr, In vivo studies of sterol and squalene secretion by human skin, J Lipid Res 15 563-573 (1974)
- F Bouvier, A Rahier and B Camara,Biogenesis, molecular regulation and function of plant isoprenoids, Prog Lipid Res 44 357-429 (2005)
- M Spanova and G Daum,Squalene—Biochemistry, molecular biology, process biotechnology and applications, Eur J Lipid Sci Technol 113 1299-1320 (2011), and references therein
- E Andre and H Canal, Contribition a l’étude des huiles d’animaux marins. I. Recherches sur le squaléne et la spinacéne, Ann ChimAppl 7 69-112 (1927)
- M Tsujimoto, An unsaturated hydrocarbon in shark liver oil, J Chem Ind Jpn 19 277-281 (1916)
- P Karrer and A Helfenstein, Synthesis of squalene,HelvChim Acta 14 78-85 (1931)
- S Sabetay, Five years of perhydrosqualene—A revolution in cosmetics, RiechstoffArom 5 274-276 (1955)
- T Nishida, Y Ninagawa, K Itoi and Y Fujita, New industrial synthesis of squalane, Bull Chem Soc Jpn 56 2805-2810 (1983)
- J Grossfeld and H Timm, A new characteristic for oliveoil, Z UntersLebensm 77 249-253 (1939)
- MT Gapor and AR Hazrina, Squalene in oils and fats, Palm Oil Develop 32 36-40 (2000)
- CA Auguet, A new source of Ssqualane, Drug Cosmet Ind 82 51-53 (1988)
- W Dickhart, The squalene contents of various oils,Am J Pharm127 359-361 (1955)
- K Taufel, H Heinisch and W Heimann, The distribution of squalenes in vegetable fats,Biochem Z 303 324-8 (1940)
- MM Storelli, E Ceci, A Storelli and GO Marcotrigiano, Polychlorinated biphenyl, heavy metal and methylmercury residues in hammerhead sharks: Contaminant status and assessment, Mar Pollut Bull 46 1035-1039 (2003)
- A Gasparoli, C Mariani and MG Fedrigucci, Squalane: Differentiation between vegetable and animal origin, Riv Ital Sostan Grasse 73 293-302 (1996)
- A.Gasparoli, CMariani, ME Gaboardi, G Morchio and G Santus, About detection of animal squalene/squalene in vegetable products used in the cosmetic field, Riv Ital Sostan Grasse 89 4-28 (2012)
- Ruzicka. The isoprene rule and the biogenesis of terpenic compounds. Experientia 9 357-67 (1953)
- F Mantzouridou and MZ Tsimidou, Observations on squalene accumulation in Saccharomyces cerevisiae due to the manipulation of HMG2 and ERG6, FEMS Yeast Res 10 699-707 (2010), and references therein
- S.S.Chandran, JT Kealey and CDReeves, Microbial production of isoprenoids, Process Biochem 46 1703-1710 (2011)
- L Zhao, W Chang, Y Xiao, HLiu and P Liu, Methylerythritol phosphate pathway of isoprenoid biosynthesis, Ann Rev Biochem 82 497-530 (2013)
